Herramientas de la Biotecnología
Entre sus herramientas tenemos:
1. LOS ANTICUERPOS MONOCLONALES
Los anticuerpos monoclonales son aquellos idénticos entre sí (clones) y que reconocen todos al mismo tipo de antígeno. El desarrollo de los anticuerpos monoclonales fue realizado por el biólogo alemán Georges Köhler y el biólogo molecular argentino Cesar Milstein en Cambridge (Inglaterra). Por este descubrimiento recibieron el premio Nobel en medicina en 1984.
Los científicos unieron células productoras de anticuerpos (linfocitos B) con células de mieloma (cancerosas). Las células híbridas se conocen como hibridomas y producen las mismas moléculas de anticuerpos, de ahí el nombre de anticuerpos monoclonales. La importancia de este desarrollo es que el hibridoma puede mantenerse indefinidamente en cultivo (contrario a lo que sucede con los linfocitos B aislados, los cuales tienen un breve período de actividad). Como consecuencia, fue posible el cultivo de células de hibridomas en fermentadores para la producción en grandes cantidades de anticuerpos específicos contra un cierto antígeno.
Los científicos unieron células productoras de anticuerpos (linfocitos B) con células de mieloma (cancerosas). Las células híbridas se conocen como hibridomas y producen las mismas moléculas de anticuerpos, de ahí el nombre de anticuerpos monoclonales. La importancia de este desarrollo es que el hibridoma puede mantenerse indefinidamente en cultivo (contrario a lo que sucede con los linfocitos B aislados, los cuales tienen un breve período de actividad). Como consecuencia, fue posible el cultivo de células de hibridomas en fermentadores para la producción en grandes cantidades de anticuerpos específicos contra un cierto antígeno.

2. ANÁLISIS DE ADN O ARN MEDIANTE PCR
Esta técnica tiene un amplio campo de aplicación en la detección de mutaciones (cambios en las secuencias de ADN) responsables de las alteraciones genéticas. Se usa corrientemente en microbiología para la identificación de patógenos virales, bacterianos y se empleará para examinar la función y regulación de genes en la investigación del cáncer.
Recientemente se ha producido una verdadera revolución en los métodos de detección de esta enfermedad, con la puesta a punto de métodos molecular Reacción en cadena de la polimerasa con transcriptasa inversa (RT-PCR del inglés Reverse transcription polymerase chain reaction) es una variante de PCR, una técnica de laboratorio comúnmente usada en biología molecular para generar una gran cantidad de copias de ADN, basados en la amplificación de ADN a partir de ARNm (el intermediario en la síntesis de proteínas). A esta técnica se la denomina PCR de transcripción reversa (RT-PCR). El procedimiento consiste en amplificar fragmentos de ARNm portadores de los mensajes genéticos para la síntesis de proteínas características de la variante tumoral en estudio. Mediante RT-PCR es posible detectar la presencia de una célula cancerosa entre un millón de células normales.

Un biosensor es un dispositivo de análisis que utiliza un ser vivo o un producto derivado de éste, habitualmente enzimas, capaces de modificar específicamente una sustancia contenida en una mezcla (sangre, orina, etc.). El compuesto modificado por la enzima se puede distinguir de distintas maneras, como por aparición de color o fluorescencia, generación de calor o por producción de algún compuesto fácil de analizar (oxígeno, agua oxigenada, etc.).

En primer lugar, un resultado positivo que confirma la presencia de anticuerpos no significa necesariamente que el paciente esté enfermo.
Recientemente se ha producido una verdadera revolución en los métodos de detección de esta enfermedad, con la puesta a punto de métodos molecular Reacción en cadena de la polimerasa con transcriptasa inversa (RT-PCR del inglés Reverse transcription polymerase chain reaction) es una variante de PCR, una técnica de laboratorio comúnmente usada en biología molecular para generar una gran cantidad de copias de ADN, basados en la amplificación de ADN a partir de ARNm (el intermediario en la síntesis de proteínas). A esta técnica se la denomina PCR de transcripción reversa (RT-PCR). El procedimiento consiste en amplificar fragmentos de ARNm portadores de los mensajes genéticos para la síntesis de proteínas características de la variante tumoral en estudio. Mediante RT-PCR es posible detectar la presencia de una célula cancerosa entre un millón de células normales.

3.CHIPS DE ADN:
Es una superficie sólida a la cual se une una colección de fragmentos de ADN. Las superficies empleadas para fijar el ADN son muy variables y pueden ser de vidrio, plástico e incluso de silicio. Los chips de ADN se usan para analizar la expresión diferencial de genes, y se monitorean de manera simultánea los niveles de miles de ellos. Su funcionamiento consiste, básicamente, en medir el nivel de hibridación entre la sonda específica (probe, en inglés), y la molécula diana (target), y se indican generalmente mediante fluorescencia y a través de un análisis de imagen, lo cual indica el nivel de expresión del gen.
Suelen utilizarse para identificar genes con una expresión diferencial en condiciones distintas. Por ejemplo, para detectar genes que producen ciertas enfermedades mediante la comparación de los niveles de expresión entre células sanas y células que están desarrollando ciertos tipos de enfermedades.

La tecnología del chip de ADN tiene su origen en una técnica muy usada en biología molecular, el Southern blot. En la era pregenómica la biología estudiaba los genes individualmente, uno a uno, por lo que los podía estudiar a fondo. Para cumplir este objetivo y poder estudiar muchos genes a la vez fue necesario un cambio de paradigma.
5. BIOSENSORES:
Los sensores enzimáticos más fáciles de utilizar y de mayor precisión contienen una enzima directamente unida a un elemento electrónico (por ejemplo, un electrodo de oxígeno) que mide la intensidad de la reacción enzimática y así determina la concentración del compuesto que se quiere analizar.
Hoy en día, se pueden obtener por biotecnología enzimas recombinantes en grandes cantidades, que resultan muy útiles para el diseño de numerosos sistemas de diagnóstico: analizadores automáticos de hospitales, tiras de diagnóstico individuales, biosensores electrónicos, etc.

Explicación de la figura: Un biosensor consiste en tres partes: un componente biológico (tejido, microorganismos, organelas, receptores celulares, enzimas, anticuerpos, ácidos nucleicos, etc.); un sistema traductor (asociado a los otros dos componentes, que traduce la respuesta biológica en una señal físico-química) y un detector (que capta la señal del traductor y la procesa)
6) La vacuna de ADN:
es una vacuna de desarrollo reciente, consistente en la inyección directa de ADN a través de un plásmido o un vector de expresión. Este ADN codifica una proteína viral antigénica de interés, que inducirá la activación del sistema inmune. De esta forma se puede inducir tanto anticuerpos neutralizantes (respuesta humoral) como inmunidad medida por linfocitos T citotóxicos (respuesta celular).
Funciona al insertar ADN de bacterias o virus dentro de células humanas o animales. Algunas células del sistema inmunitario reconocen la proteína surgida del ADN extraño y atacan tanto a la propia proteína como a las células afectadas. Dado que estas células viven largo tiempo, si el agente patógeno (el que crea la infección), que normalmente produce esas proteínas, es encontrado tras un periodo largo, serán atacadas instantáneamente por el sistema inmunitario. Una ventaja de las vacunas ADN es que son muy fáciles de producir y almacenar. Este tipo de vacuna comenzó a conocerse en la década de 1990 y todavía hoy, en 2011, continúan realizándose numerosos estudios dentro del campo de la experimentación. Aunque no son de uso clínico por el momento, sus expectativas son muy prometedoras. La manera de aplicar estas vacunas podría ser a través de liposomas (en cremas), inyecciones o a través de biobalística.
6) La electroforesis:
es una técnica para la separación de moléculas según la movilidad de éstas en un campo eléctrico. La separación puede realizarse sobre la superficie hidratada de un soporte sólido (p. ej., electroforesis en papel o en acetato de celulosa), a través de una matriz porosa (electroforesis en gel), o bien en disolución (electroforesis libre). Dependiendo de la técnica que se use, la separación obedece en distinta medida a la carga eléctrica de las moléculas y a su masa.
La electroforesis se usa en una gran mayoría en la materia del ADN recombinante ya que nos permite saber la carga que poseen los polipéptidos, y separar los diferentes polipeptidos resultantes de las variaciones del experimento del ADN recombinante. La variante de uso más común para el análisis de mezclas de proteínas o de ácidos nucleicos utiliza como soporte un gel, habitualmente de agarosa o de poliacrilamida. Los ácidos nucleicos ya disponen de una carga eléctrica negativa, que los dirigirá al polo positivo, mientras que las proteínas se cargan al unirse con sustancias como el SDS (detergente) que incorpora cargas negativas de una manera dependiente de la masa molecular de la proteína. Al poner la mezcla de moléculas y aplicar un campo eléctrico, éstas se moverán y deberán ir pasando por la malla del gel (una red tridimensional de fibras cruzadas), por lo que las pequeñas se moverán mejor, más rápidamente. Así, las más pequeñas avanzarán más y las más grandes quedarán cerca del lugar de partida.
La gran mayoría de macromoléculas están cargadas eléctricamente y, al igual que loselectrolitos, se pueden clasificar en fuertes y débiles dependiendo de la constante de ionización de grupos ácidos y básicos.
(acrónimo delinglés Enzyme-Linked ImmunoSorbent Assay: ‘ensayo por inmunoabsorción ligado a enzimas’) es una técnica deinmunoensayo en la cual unantígeno inmovilizado se detecta mediante un anticuerpoenlazado a una enzima capaz de generar un producto detectable, como cambio de color o algún otro tipo; en ocasiones, con el fin de reducir los costos del ensayo, nos encontramos con que existe un anticuerpo primario que reconoce al antígeno y que a su vez es reconocido por un anticuerpo secundario que lleva enlazado la enzima anteriormente mencionada. La aparición de colorantes permite medir indirectamente mediante espectrofotometría el antígeno en la muestra.
Se usa en muchos laboratorios para determinar si un anticuerpo particular está presente en la muestra de sangre de un paciente. Aunque el procedimiento es rutinario y sencillo, involucra a un gran número de variables, tales como selección de reactivo, temperatura, medición de volumen y tiempo, que si no se ajustan correctamente, puede afectar los pasos sucesivos y el resultado de la prueba.
La interacción antígeno-anticuerpo en el laboratorio puede ser utilizada para determinar si un paciente tiene una infección o una enfermedad autoinmune. Pero como prueba diagnóstica, posee diversas limitaciones que conviene conocer:
En primer lugar, un resultado positivo que confirma la presencia de anticuerpos no significa necesariamente que el paciente esté enfermo.
En segundo lugar, hay personas que producen una baja cantidad de anticuerpos, por lo que estos pueden pasar desapercibidos y no ser medidos, dando lugar a un falso negativo.
8) Inmunoprecipitación de Cromatina (ChIP):
La estructura de la cromatina desempeña un papel fundamental en la función del ADN. Regula procesos que se dan sobre la estructura nucleosomal como la transcripción, la replicación y la recombinación. Por lo tanto, determinar la distribución de las modificaciones específicas de las histonas y sus variantes, así como la de otros componentes de la cromatina sobre en secuencias específicas del ADN puede proporcionar información valiosa acerca de cómo funcionan estas proteínas (y sus modificaciones) dentro del contexto de la cromatina.
La Inmunoprecipitación de Cromatina (ChIP) es un método bioquímico usado principalmente para determinar la localización en el genoma de histonas modificadas y de otras proteínas in vivo. También se emplea para estudiar la unión de factores de transcripción al ADN. Esta técnica consiste en el uso de unanticuerpo que reconozca la proteína de interés no solamente en disolución sino también en la cromatina.
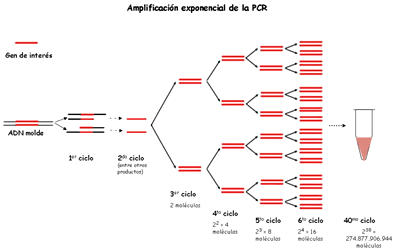
9) La reacción en cadena de la polimerasa:
conocida como PCR por sus siglas en inglés (polymerasechain reaction), es una técnica de biología moleculardesarrollada en 1986 por Kary Mullis,1 .Su objetivo es obtener un gran número de copias de un fragmento de ADN particular, partiendo de un mínimo; en teoría basta partir de una única copia de ese fragmento original, o molde.
Esta técnica sirve para amplificar un fragmento de ADN; su utilidad es que tras la amplificación resulta mucho más fácil identificar con una muy alta probabilidad, virus o bacterias causantes de unaenfermedad, identificar personas (cadáveres) o hacer investigación científica sobre el ADN amplificado. Estos usos derivados de la amplificación han hecho que se convierta en una técnica muy extendida, sobre todo en el ámbito de la investigación forense, con el consiguiente abaratamiento del equipo necesario para llevar a cabo dicha técnica.
Esta técnica se fundamenta en la propiedad natural de los ADN polimerasas para replicar hebras de ADN, para lo cual se emplean ciclos de altas y bajas temperaturas alternadas para separar las hebras de ADN recién formadas entre sí tras cada fase de replicación y, a continuación, dejar que las hebras de ADN vuelvan a unirse para poder duplicarlas nuevamente. La reacción en cadena de la polimerasa fue perfeccionada por Kary Mullisperteneciente a la Cetus Corporation en California, en la década de 1980.Hoy, todo el proceso de la PCR está automatizado mediante un aparato llamado termociclador,
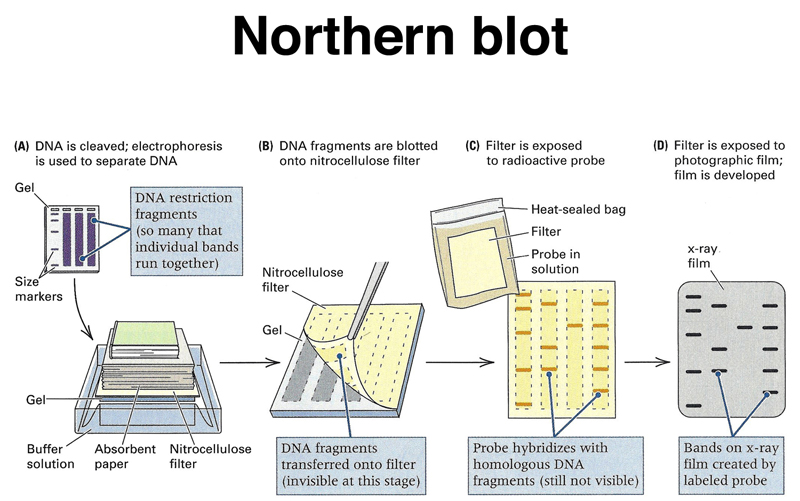
Hibridación northern o ensayo northern es una técnica de detección de moléculas de ácido ribonucleico (ARN) de una secuencia dada dentro de una mezcla compleja (por ejemplo, un ARN mensajero para un péptido dado en una muestra de ARN total). Para ello, se toma la mezcla de ARN y se somete a una electroforesis en gel a fin de separar los fragmentos de acuerdo con su tamaño. Tras esto, se transfiere el contenido del gel, ya resuelto, a una membrana cargada positivamente en la que se efectúa la hibridación de una sonda molecular marcada radiactiva o químicamente.
El nombre de la técnica deriva de la que detecta ácido desoxirribonucleico (ADN), denominada Southern blot en honor a su inventor, Edwin Southern (1975). En 1977, James Alwine, David Kemp y George Stark en la Universidad de Stanford desarrollaron el northern blot y lo denominaron empleando el punto cardinal opuesto («northern», septentrional en inglés, frente al meridional «southern»).
El procedimiento general comienza con la extracción del ARN total de una muestra de tejido homogeneizado. El ARNm se puede aislar mediante cromatografía para retener solamente los ARN con colas de poli(A). Las muestras de ARN se separan entonces medianteelectroforesis en gel. Dada la fragilidad de los geles y la dificultad para que las sondas penetren en la matriz, las muestras de ARN, separadas por tamaño tras la electroforesis, se transfieren a una membrana de nailon, bien por capilaridad o empleando un sistema de vacío.